23 / 12 / 30
医药观察 #20:再看布地奈德治疗 IgA 肾病
两年前,美国食品药品监督管理局(FDA)有条件批准布地奈德(budesonide)治疗原发性 IgA 肾病(IgA nephropathy),我曾撰文聊过这个“老药新用 ”。如今其 3 期临床试验(NefIgArd 研究 )进一步结果发表,我们得以一窥该药的实际临床获益。
之前 FDA 的批准依据是布地奈德能够降低蛋白尿水平,但 IgA 肾病患者面临的首要问题始终是肾脏功能持续缓慢恶化,一旦到达终末阶段依赖血液透析才能生存。NefIgArd 研究试图证明的临床获益,就是布地奈德对肾脏功能的长期影响。
简要回顾 NefIgArd 研究的设计:试验参与者随机分为两组,一组接受 9 个月(“治疗期”)布地奈德治疗,一组接受同样时长的安慰剂,治疗结束后继续接受 15 个月(“随访期”)定期检查;前后相加共两年时间。为了比较两组患者的肾脏功能,试验选择估算肾小球滤过率(eGFR )作为观察指标。肾小球滤过率(GFR)可以客观反映人体肾脏功能,但由于测定方法复杂、成本昂贵,临床工作中往往使用血液检查结果、年龄、性格、身高、体重等参数,估算近似值 eGFR。
试验随访期末(即治疗开始两年后),布地奈德组患者 eGFR 的下降幅度显著低于安慰剂组,表明布地奈德在治疗开始后两年内能够减缓 IgA 肾病患者的肾脏功能恶化,确有临床获益。(Lafayette et al. 2023) 根据这一结果,FDA 也 正式批准该药上市 。
不过仔细观察试验参与者的 eGFR 变化曲线(见下图),会发现有趣现象。安慰剂组患者的 eGFR 从治疗开始即稳定下降,而布地奈德组患者治疗最初 3 个月 eGFR 不降反增,随后才开始稳定下降——两组 eGFR 曲线 3 个月后的下降速度几乎一致。根据文章数据,两组 eGFR 每年下降幅度差粗算约 0.6 mL/min/1.73 m2。相比从治疗开始时计算的 eGFR 每年下降幅度差(2.95 mL/min/1.73 m2),明显缩窄。换言之,布地奈德组患者两年来的肾脏功能获益,很大一部分来自治疗最初 3 个月。
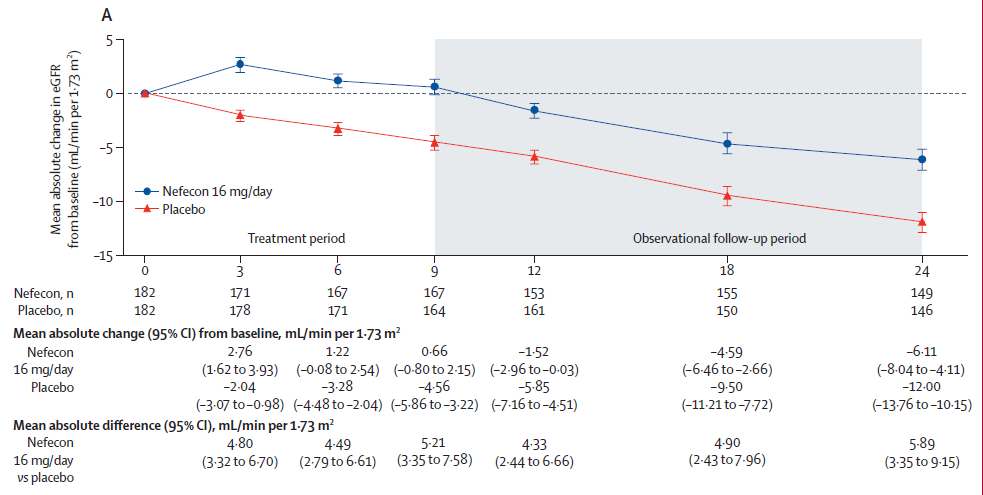
eGFR 变化斜率终点得到了美国和欧盟药物监管机构的认可,立场偶尔不同:比如内皮素 A 受体(ETAR)、血管紧张素 Ⅱ 1 型受体(AT1R)阻断药物 sparsentan,其局灶节段性肾小球硬化(FSGS)3 期临床试验(DUPLEX 研究 )允许采用 eGFR 斜率终点评估临床获益——只是 FDA 要求总斜率,EMA 要求慢性斜率 。
这类替代终点终究有局限:受临床试验观察时间影响,只能反映观察期间的获益,无法确定更久远的临床结局。回到布地奈德的例子,IgA 肾病患者在治疗开始两年内获益,两年后呢?从上图看,布地奈德组患者第 10 个月 eGFR 回到治疗前水平。假如治疗 3 个月后,布地奈德和安慰剂组患者的 eGFR 下降速度实际相当,是不是说明布地奈德治疗患者最终仍将进入终末期,只不过比不接受布地奈德治疗的患者平均晚 10 个月?
我们看看类似药物的表现,如甲泼尼龙(methylprednisolone)。相比布地奈德这种作用范围较小的糖皮质激素,甲泼尼龙口服吸收后全身血液都有分布,被称作全身性(systemic)糖皮质激素。在 IgA 肾病临床试验(TESTING 研究 )中,甲泼尼龙治疗 6-8 个月,治疗开始至第 3 年末的 eGFR 变化趋势(见下图)与 NefIgArd 研究如出一辙,治疗最初 3 个月反跳,随即逐渐降低。甲泼尼龙组患者 eGFR 下降速度似乎略低,但总体接近安慰剂组患者。(Lv et al. 2017)
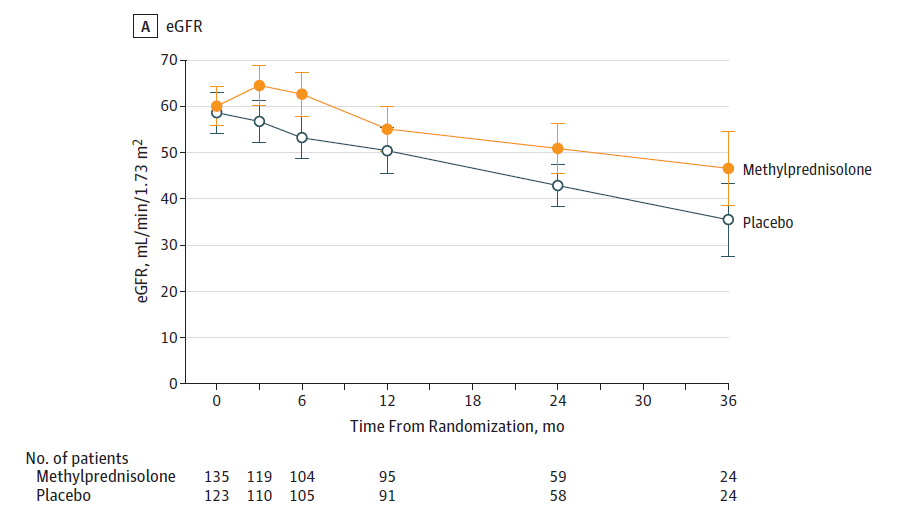
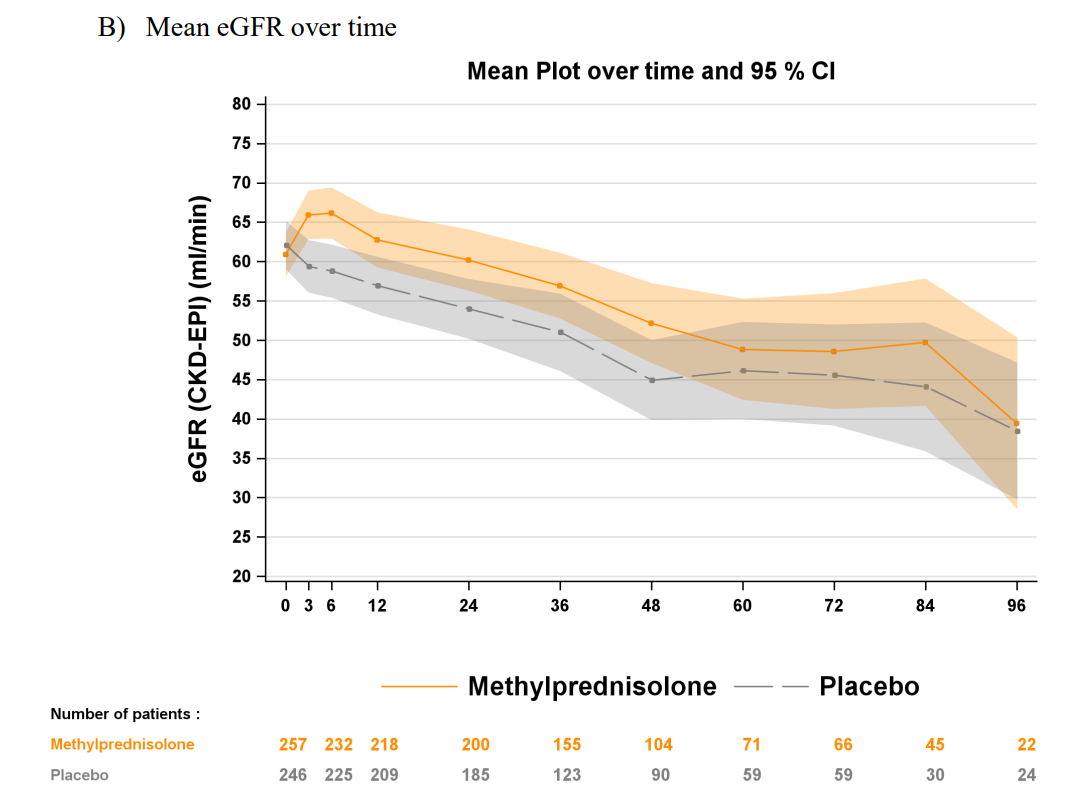
布地奈德和 NefIgard 研究对 IgA 肾病患者意义重大,但其中产生的问题值得我们追问:蛋白尿水平作为替代终点是否合理?毕竟布地奈德组患者蛋白尿水平持续控制,肾功能却仍不断降低,速度与安慰剂组相似。布地奈德当前治疗方案是否可以优化?缩短 9 个月治疗期,或间断给药,也许能获得更佳临床获益、更少不良反应。IgA 肾病除了肠道派尔淋巴结(Peyer’s patch ),是否还有其他淋巴结需要干预……IgA 肾病新药研发活跃的今天,我们完全有理由期待这些问题得到解答。
利益冲突:笔者单位正在开发 IgA 肾病药物。本文仅代表个人观点,与工作单位无关。
参考文献
Inker, Lesley A., Hiddo J. L. Heerspink, Hocine Tighiouart, Andrew S. Levey, Josef Coresh, Ron T. Gansevoort, Andrew L. Simon, et al. 2019. “GFR Slope as a Surrogate End Point for Kidney Disease Progression in Clinical Trials: A Meta-Analysis of Treatment Effects of Randomized Controlled Trials.” Journal of the American Society of Nephrology 30 (9): 1735–45.
Lafayette, Richard, Jens Kristensen, Andrew Stone, Jürgen Floege, Vladimir Tesař, Hernán Trimarchi, Hong Zhang, et al. 2023. “Efficacy and Safety of a Targeted-Release Formulation of Budesonide in Patients with Primary IgA Nephropathy (NefIgArd): 2-Year Results from a Randomised Phase 3 Trial.” The Lancet 402 (10405): 859–70.
Lv, Jicheng, Muh Geot Wong, Michelle A. Hladunewich, Vivekanand Jha, Lai Seong Hooi, Helen Monaghan, Minghui Zhao, et al. 2022. “Effect of Oral Methylprednisolone on Decline in Kidney Function or Kidney Failure in Patients With IgA Nephropathy: The TESTING Randomized Clinical Trial.” JAMA 327 (19): 1888.
Lv, Jicheng, Hong Zhang, Muh Geot Wong, Meg J. Jardine, Michelle Hladunewich, Vivek Jha, Helen Monaghan, et al. 2017. “Effect of Oral Methylprednisolone on Clinical Outcomes in Patients With IgA Nephropathy: The TESTING Randomized Clinical Trial.” JAMA 318 (5): 432.