CLARITY AD 研究是阿尔茨海默病药物 lecanemab 的 3 期临床试验,一个月前在学术会议上公布了详细数据,论文也同期发表 (van Dyck et al. 2022)。围绕试验结果的讨论至今仍在继续,焦点一直是所有药物的最基本属性:临床疗效、安全风险。
“CLARITY”意为“清晰”,如愿得到确切的统计学显著疗效结果。在针对 β 淀粉样蛋白(amyloid beta)的药物前仆后继开发失败的当下,lecanemab 成为其中唯一通过完整疗效验证临床试验(confirmatory trial)的分子,大家自然急于知道,如果 lecanemab 确实有效,它做对了什么?
一种声音是 lecanemab 找对了干预目标。阿尔茨海默病的 β 淀粉样蛋白假说,涉及从 β 淀粉样蛋白前体(precursor)到最终聚集形成病理性斑块(plaque)的多种成分,理化性质、生理作用各异(见下图,图片来源)。各种药物虽然针对的都是 β 淀粉样蛋白假说,但其作用细化 干预的是不同成分。譬如去年批准上市、备受争议的 aducanumab 作用于 β 淀粉样蛋白的寡聚体(oligomer)和原纤维(fibril);刚刚宣布 3 期临床试验失败的 gantenerumab 作用于原纤维和斑块;预计明年公布 3 期临床试验结果的 donanemab 为斑块“量身定制”。而 lecanemab 的设计初衷是作用于寡聚体和原纤维当中的初纤维(protofibril)阶段。
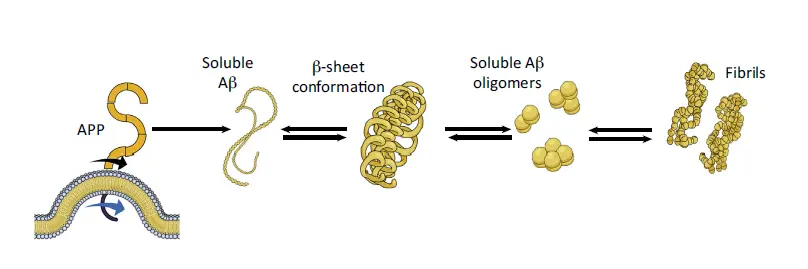
然而这些药物的目标多少有些交集,并不是非此即彼、完全独立的关系。β 淀粉样蛋白的各个阶段也终究是连续过程,即使 lecanemab 的目标是唯一正解,针对其上游成分的药物对下游不可能毫无影响。通过药物目标的细微差异解释 lecanemab 在 β 淀粉样蛋白药物中脱颖而出,难以令人信服。
随着近几年 β 淀粉样蛋白示踪剂(tracer)广泛应用,各类药物临床试验数据积累,以及早期开发阶段陆续观察到疗效苗头,另一种更加简明直观的解释发展起来:β 淀粉样蛋白药物的疗效,是大脑 β 淀粉样蛋白斑块清除的结果 (Karran and De Strooper 2022)。CLARITY AD 研究中,试验剂量的 lecanemab 大量清除了大脑 β 淀粉样蛋白斑块。去年美国食品药品监督管理局(FDA)临床药理学办公室将 6 个抗 β 淀粉样蛋白单克隆抗体(monoclonal antibody)的临床试验数据放在一起分析,曾得到 类似结论(见下图),并作为支持 aducanumab 上市的依据。
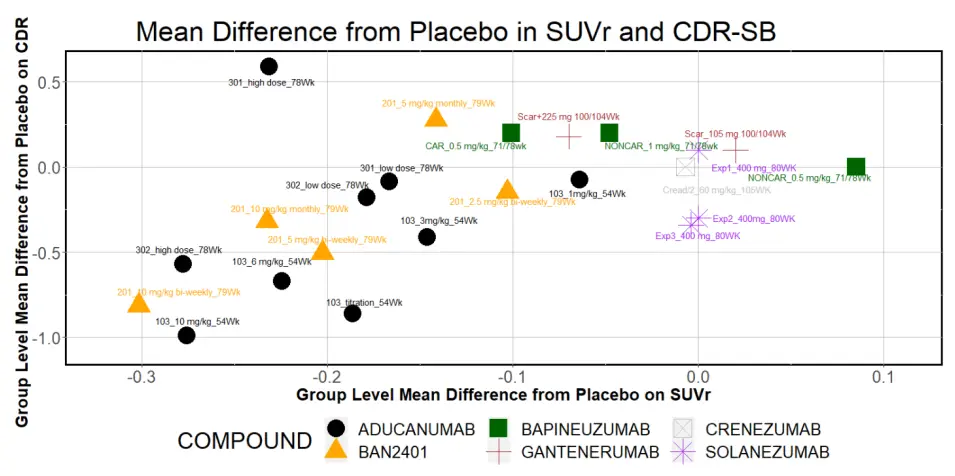
这套理论描述了“lead and lag”现象,即药物临床疗效会晚于 β 淀粉样蛋白斑块清除一段时间显现出来。换言之,理想的抗 β 淀粉样蛋白药物必须快速、彻底地清除 β 淀粉样蛋白斑块,这样观察时间有限的临床试验才有可能观察到足够的临床疗效。而二十年屡战屡败的 gantenerumab 成了这套理论的完美反例,它需要剂量逐渐增加,经过漫长 9 个月时间才能达到目标剂量, 最新的 3 期临床试验持续用药 2 年 β 淀粉样蛋白清除效果低于预期。
不过这套理论目前依据有限。早期几种 β 淀粉样蛋白单克隆抗体对大脑斑块没有影响,放在一起分析意义不大。之后 aducanumab 的临床试验支离破碎,又按剂量组拆分,结果是否可靠令人存疑。CLARITY AD 研究的 部分亚组分析结果与 β 淀粉样蛋白假说推论相悖,也给许多人理由观望。
相比药物起效机制,CLARITY AD 临床试验观察到的疗效对临床医生是否足够(即“具有临床意义”),倒没有那么重要了。CLARITY AD 研究选择的临床痴呆量表( Clinical Dementia Rating, CDR)可以同时评估患者认知水平和日常功能,符合 FDA 推荐,成为许多同类临床试验的疗效指标。但 CDR 相差多少分才意味着临床意义,尚无公论。好在这一问题可以通过长期治疗结果解答。CLARITY AD 研究 lecanemab 组和安慰剂组治疗 18 个月,总分 18 分的 CDR 评分绝对值组间仅差 0.45 分,似乎微不足道,但转换为相对差异 lecanemab 组改善了 27%。假如 lecanemab 的疗效能够长期维持同一水平,出现具有临床意义的疗效不过是时间问题(及费用问题)。
提到 lecanemab 的安全风险,重点仍是 淀粉样蛋白相关影像学异常(amyloid-related imaging abnormalities, ARIA)。CLARITY AD 研究接受 lecanemab 治疗的受试者,约 12.6% 发生水肿、渗出型 ARIA(ARIA-E),其中近四分之一出现症状;约 17.3% 发生出血或含铁血红素沉积型 ARIA(ARIA-H),其中不到 5% 出现症状。试验中无 ARIA 事件导致受试者死亡,临床性质也符合既有认知。然而不时报道的 极端病例,迫使医学界必须保持审慎。此外,也有人注意到 lecanemab 早期临床试验受试者脑体积降低,只是还无法确定实际意义。
CLARITY AD 疗效结果“清晰”,却仍有许多不清晰之处等待解答。类似的早期阿尔茨海默病大规模临床试验耗时久、成本高,制药企业想必不愿重复。我们只能期望仍在进行的其他临床试验,能带给我们更丰富的数据:donanemab 的 3 期临床试验 结果,或许可以验证斑块清除是否确实产生临床疗效;CLARITY AD 研究的延长治疗期结果,或许可以证实 lecanemab 的疗效是否持久、稳定;阿尔茨海默病预防试验 AHEAD3-45 结果,或许可以探索早期干预的更大获益机会。至于依靠 Brain Shuttle 技术延续生命的 gantenerumab,我们或许可以见识新药研究开发工作者的倔强。
参考文献
- Dyck, Christopher H. van, Chad J. Swanson, Paul Aisen, Randall J. Bateman, Christopher Chen, Michelle Gee, Michio Kanekiyo, et al. 2022. “Lecanemab in Early Alzheimer’s Disease.” New England Journal of Medicine, November, NEJMoa2212948.
- Karran, Eric, and Bart De Strooper. 2022. “The Amyloid Hypothesis in Alzheimer Disease: New Insights from New Therapeutics.” Nature Reviews Drug Discovery 21 (4): 306–18.