脊髓性肌萎缩症(spinal muscular atrophy,简称 SMA)药物 branaplam,由于市场竞争格局终止开发。不久开发工作重新启动,只是适应症变成了亨廷顿舞蹈病(Huntington’s disease,简称 HD),还获得美国食品药品监督管理局(FDA)的 孤儿药、快速审批通道 资质。开发企业近日发表学术文章,介绍 branaplam 重定位适应症(repurpose)的科学依据 (Keller et al. 2022),或可一窥成熟医药研发企业开发决策的途径。
根据文章内容,branaplam 治疗 SMA 的机制,与已上市 SMA 药物 risdiplam 类似:通过影响特定基因(SMN2)的剪接(splicing)过程,帮助患者合成体内缺乏的必要蛋白质。然而研究人员发现,除了 SMN2 基因,branaplam 还可以改变另一种基因 HTT 的剪接模式,减少对应蛋白质生成。HD 目前公认的病因,正是突变 HTT 基因产生了大量对人体有害的蛋白质。branaplam 干预 HTT 基因剪接,同样波及突变基因产生的有害蛋白质,理论上具备治疗 HD 的可能性。
这两种药物实现疗效的生理基础,是许多生物体内普遍存在的 RNA 选择性剪接(alternative splicing)现象。一段基因剪接时,会有选择地将其中不同片段连缀起来,形成不同 mRNA,生成不同蛋白质(如下图,图片来源:Wikipedia)。通过“选择性剪接”,同一段基因能够对应生产几种蛋白质,大大丰富了生物的蛋白质种类,也 引起一些疾病。
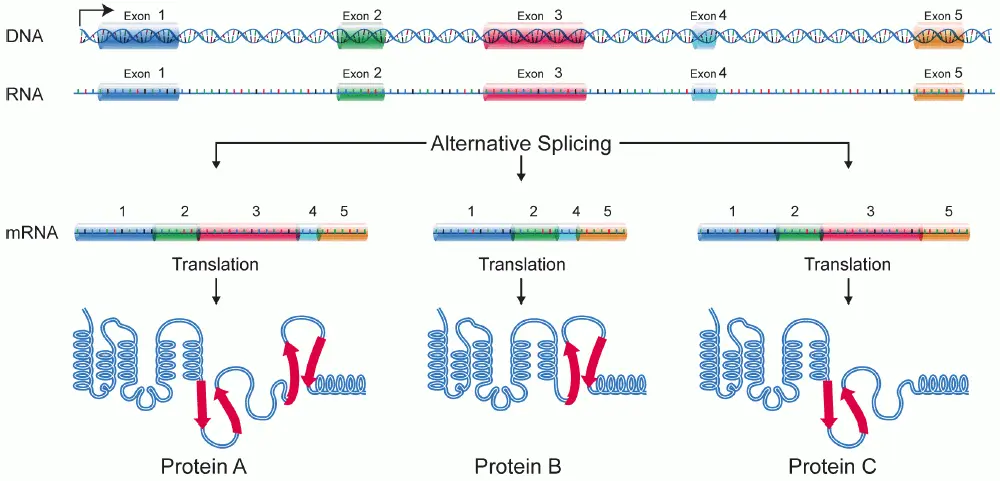
口服化学小分子药物介入 RNA 层面时间不长,risdiplam 是第一款获得上市批准的 RNA 剪接药物。包括 branaplam 极有可能与剪接蛋白质(剪接过程里的“剪刀”和“胶水”)协作发挥效力 (Ratni, Scalco, and Stephan 2021)。有趣的是,两者都通过增加特定蛋白质来治疗 SMA,但前者却通过降低特定蛋白质治疗 HD——branaplam 为这类药物的实际应用拓展了可能。
虽然研究人员在体外、动物试验中观察到 branaplam 降低 HD 有害蛋白的效果,但促使企业下决心再投重金、重启 branaplam 开发,文章当中篇幅不大的一段数据恐怕才是关键推手。他们检测了来自 branaplam 早期 SMA 临床研究受试者的血液样本,发现负责有害蛋白生产的 mRNA 确实减少了。在目标患者人群开始试用新药前,就足以验证理论的人体数据弥足珍贵,意味着临床试验更可能成功,大大强化了企业的信心。SMA 临床试验受试者的血液样本,用在原来研究目的不一致的地方,为另一种严重的罕见病患者带来希望。
我曾工作过的跨国制药企业、我正合作的跨国制药企业,都维护着各自的生物样本库,专门从临床研究中收集受试者额外的血液样本等,主要目的是为了寻找新的诊断指标、开发新的治疗方法、探索新的疾病特征。我也见过企业将样本库检测结果捐给国际科研组织,构建更庞大、全面的疾病数据库,与全球研究者一同推进医药研究。branaplam 的故事只是其中一例。
从此可以看出,中国生物医药企业近年蓬勃发展,但与医药研发领域的国际巨头仍有明显差距。一方面,采集、储藏额外样本耗费巨大;另一方面,分析这些样本,既需要深厚的技术积累,又离不开本土企业研究人员对疾病、药物方方面面的敏锐洞察。国内绝大多数生物医药企业资源有限,罕有挑战新疾病、新靶点的决心,更别提国内对人体样本矫枉过正、近乎死板的管理政策了。
相比之前“纸上谈兵式的老药新用”,branaplam 案例无疑更接近真实世界的药物开发逻辑。希望愈加成熟的技术,可以为人类带来更多类似的药物重启机会。
参考文献
- Keller, Caroline Gubser, Youngah Shin, Alex Mas Monteys, Nicole Renaud, Martin Beibel, Natalia Teider, Thomas Peters, et al. 2022. “An Orally Available, Brain Penetrant, Small Molecule Lowers Huntingtin Levels by Enhancing Pseudoexon Inclusion.” Nature Communications 13 (1): 1150.
- Ratni, Hasane, Renata S. Scalco, and Alexander H. Stephan. 2021. “Risdiplam, the First Approved Small Molecule Splicing Modifier Drug as a Blueprint for Future Transformative Medicines.” ACS Medicinal Chemistry Letters 12 (6): 874–77.