从传出 断供、停产消息,到证实 中国药品监督管理局(NMPA)拒绝延长上市许可,短短数月,饱受争议的阿尔茨海默病(Alzheimer's disease)药物“九期一”(甘露特纳,俗称 GV-971)上市之路暂告一段落。有人视之为“拨乱反正”,在我看来却是制药企业、监管机构最体面的收场。
再次感谢言西邀请录制 播客,让我有机会回顾这款上市时有多瞩目、就有多争议的国产创新药。其争议集中在药物作用机制和中国 3 期临床试验两方面。

九期一宣称通过影响“脑肠轴”发挥治疗阿尔茨海默病的作用。具体而言,九期一能够平衡肠道菌群,抑制神经系统内的炎症反应,降低阿尔茨海默病相关毒性蛋白数量,从而产生疗效(如下图所示,图片出处)。
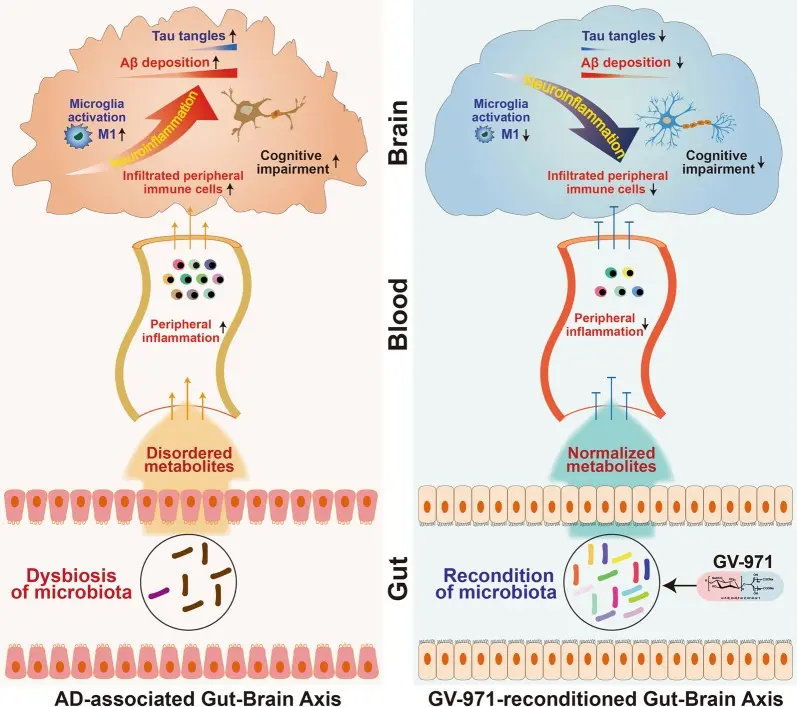
这套理论并非毫无依据,但证据级别、受认同程度,都不及 β 淀粉样蛋白(amyloid β) 等假说主流。由于缺乏早期研究数据铺垫,九期一带着陌生的作用机制,突然在新药研究开发失败率极高的阿尔茨海默病领域崭露头角,自然像“无源之水”、从石头里蹦出来的科学突破。无怪乎当时大量声音质疑其理论基础,其中不乏时任首都医科大学校长的知名科学家饶毅教授(2020 年,2022 年)这样的重量级科学家——这倒引发了我的深思:面对非主流假说,学界是否应只停留在“纸上谈兵”式的质疑,或应积极组织临床资源验证?
然而阿尔茨海默症本身极为复杂,我们至今不清楚其致病原因,同时存在多种假说,如 β 淀粉样蛋白、tau 蛋白、糖代谢、感染、免疫、重金属……即使现在针对 β 淀粉样蛋白的药物获得了一些证据,但有限的疗效暗示阿尔茨海默病可能是多因素共同作用的结果,其他假说仍占有一席之地。九期一“脑肠轴”涉及的肠道菌群是 众多假说之一,无法断言其必然错误,还需积累更多研究数据。
第二个争议点,则是九期一在国内开展的 3 期临床试验(NCT02293915)。这一随机双盲研究提供了本品的关键疗效信息,共招募 818 名轻至中度阿尔茨海默病患者,接受九期一或安慰剂治疗 36 周(约 9 个月),主要疗效指标是经典的 ADAS-Cog12 认知量表 评分(总分 80 分)。最终结果表明九期一治疗人群相比安慰剂人群观察到统计学显著的认知改善(两组差异 2.54 分)。研究委托了国际一线的合同研究组织(CRO)IQVIA 执行,国内多位阿尔茨海默病领域知名专家参与,疗效评估流程也遵照国际标准。在无确凿证据证明研究数据造假前,我倾向认同这项研究结果基本可靠(无法排除假阳性可能)。
无奈这项临床试验先天不足:
- 患者人群:试验招募患者主要依据临床表现诊断阿尔茨海默病,未参考脑脊液、PET 等病理学诊断方法,这与中国主流的阿尔茨海默病诊疗习惯一致,却无法避免混杂非阿尔茨海默病的痴呆(dementia)患者,降低试验结果针对特定疾病的适用性。
- 治疗时间:36 周治疗期过短,难以区分药物究竟仅限于改善临床症状(即对症药物),还是能真正影响疾病生理基础,实现长期有效;新机制阿尔茨海默病研究的治疗时间,一年或更长时间是必要的。
- 疗效指标:主要疗效仅包括认知评分,未评估日常生活功能。目前 中国、美国 的阿尔茨海默病药物临床试验指导原则均推荐同时考察认知和日常生活功能(或总体状态),后者对患者更具实际意义。该研究次要疗效指标有日常功能等,可惜未观察到与主要疗效指标相匹配的获益。
- 机制验证:九期一引入了证据不足的“脑肠轴”机制,3 期临床试验却缺少对应的验证方法,未能证实药物按照设想的作用机制发挥治疗效果。
可问题在于,这些瑕疵是否严重到影响临床试验结果可信度的地步?答案是“未必”:临床诊断阿尔茨海默病的痴呆患者,接受 9 个月药物治疗后,相比安慰剂患者,认知量表出现统计学显著的临床疗效,这样的结果并不特别,因为对症药物(如多奈哌齐、美金刚胺)都可能做到这一点。
如果我们承认临床试验作为裁定药物疗效的金标准,而中国法规对 3 期临床试验的数量没有专门要求,同时理解中国药物监管机构对本国创新药事业的扶持态度,当初九期一的“有条件批准上市”,无疑是可以接受的。作为上市条件,监管机构也要求制药企业计划必须开展验证疗效的临床试验——即后来的国际多中心 3 期临床试验(NCT04520412),原计划在中国、美国、欧洲招募共 2046 名患者,遗憾的是 2022 年 5 月提前终止。
这个决定是不是早有预谋?不知道,但根据我的经验,一项阿尔茨海默病的国际多中心 3 期临床试验,计划招募两千余患者,治疗两年,预算和风险根本不是普通药企能够承担的。研究设计方面,我从企业内部知情人处知晓,国际多中心临床试验虽然采纳了生物标志物诊断,但仍未尝试在临床上验证九期一机制。这一缺失,使其理论基础始终停滞在“假说”层面,无法得到临床数据的有力支持。
最终九期一未能在上市许可延期前完成疗效验证研究,所以中国药物监管机构拒绝延期——九期一退市成了另一个合情合理的决定。这不一定是九期一的结局,据传绿谷已经在中国境内重新开展疗效验证研究。如果结果有利,药物当然可以重新获批上市。
由于国内一贯的不透明决策(监管机构未公开药品审评报告),以及关注八卦信息的趋势(比如企业创始人吕松涛的经历),过去几年针对九期一的争论大多无法切中肯綮,对于药物的机制疗效、脑肠轴在阿尔茨海默病中的实际位置(如果你对前沿感兴趣,可以从 这篇文章 开始),缺乏有价值的讨论和验证,这是尤其令人唏嘘的地方。药物研发当然应该遵循科学规范,但我们同样应对未经证实(或证伪)的科学假说足够宽容。实事求是地尊重科学逻辑、证据,才能鼓励更多人深入探索复杂的疾病问题。
最后提醒大家:阿尔茨海默病是一种 可以预防 的疾病 (Livingston et al. 2024):健康饮食、规律运动、良好睡眠、积极社交、戒烟控酒……维护自己的大脑健康,认真地生活,远比网络论战有意义!
参考文献
- Livingston, Gill, Jonathan Huntley, Kathy Y Liu, Sergi G Costafreda, Geir Selbæk, Suvarna Alladi, David Ames, et al. 2024. “Dementia Prevention, Intervention, and Care: 2024 Report of the Lancet Standing Commission.” The Lancet, July, S0140673624012960.